Během posledních deseti let proběhlo mnoho úspěšných pozorování v této oblasti. Ačkoli počet publikací o použití OV výrazně stoupá, zdá se, že v České republice tato oblast nevyvolala zvláštní zájem s výjimkou nedokončené klinické studie společnosti SOTIO a. s., která využívala OV ONCOS-102. Viroterapie nádorů má dlouhou historii, která vedla od náhodných pozorování, kdy virová infekce nebo vakcinace oslabenými viry může zlepšit stav pacientů s rakovinou, až po současné sofistikované přístupy využívající různé viry a infikované buňky. Přesto není zcela jasné, jaké konkrétní mechanismy přispívají k úspěchu této terapie. Termín „onkolytický virus“ naznačuje, že virus selektivně napadá a ničí nádorové buňky, ale existují i další možnosti, například schopnost ničit nádorovou cévní síť a působit jako antiangiogenní činidlo. Je však stále zřejmější, že úspěch OV spočívá v jejich schopnosti indukovat imunitní smrt nádorových buněk a vyvolat protinádorovou imunitu různými způsoby, které lze ještě posílit pomocí cílených modifikací.
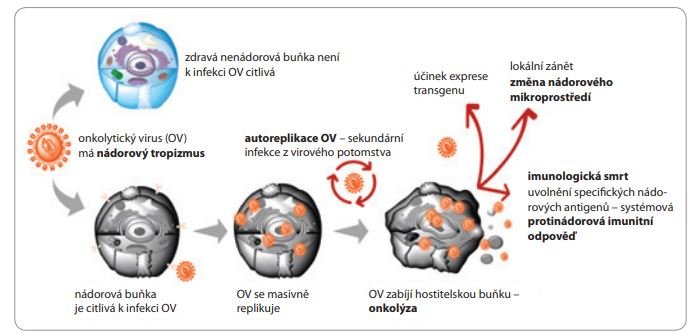
Použití onkolytických virů (OV) v léčbě nádorů je vnímané především jako forma protinádorové imunoterapie s výhodou, že OV se dokáže v nádorech množit a šířit samovolně. Na rozdíl od protinádorových vakcín nemusí OV nést specifický antigen, protože tumor-specifické antigeny jsou uvolňované při rozpadu buněk indukovaném virem. Proto se pro léčbu OV často používá termín „viroimunoterapie“. Prvním OV schváleným pro klinické použití v euroatlantickém prostoru je talimogene laherparepvec (T-VEC), prodávaný pod obchodním názvem ImlygicTM. Jedná se o geneticky upravený virus herpes simplex 1 (HSV-1), který produkuje imunostimulant granulocyte-macrophage colony stimulating factor (GM-CSF) a aplikuje se přímo do nádorů při léčbě rekurentního melanomu.
Zajímavé výsledky se zaznamenaly i při použití OV jako adjuvans protinádorových vakcín, kde efekt OV nebyl závislý na množení viru v nádorových buňkách. Schopnost OV přinášet do nádoru další signály nebezpečí a měnit imunologicky restriktivní „chladné“ nádorové mikroprostředí na imunologicky „horké“ prozápalové místo, které je citlivé na aditivní kombinovanou (imuno)terapii, se stává nejčastějším předmětem probíhajících klinických studií s velmi povzbudivými výsledky. Vývoj nových OV s přesně navrženými úpravami pro zvýšení jejich účinnosti stále pokračuje a přináší velmi zajímavé výsledky. Tato přehledová práce shrnuje obě oblasti: první část se zabývá otázkami vývoje a výběru OV, zatímco druhá část je věnována převážně klinickému použití OV u konkrétních nádorů. Druhé části se budeme věnovat v dalším článku.
Ideální Strategie vývoje onkolytických virů (OV) se zaměřuje na dosažení ideálního OV, který by neměl způsobovat žádné onemocnění u pacienta. Při infekci by měl preferovat nádorové buňky před normálními buňkami. Účinná infekce nádoru by neměla být omezená antivirovou odpovědí, například přítomností protilátek. Současně by měl OV indukovat imunogenní formu smrti všech rakovinných buněk, což by vedlo k silné, systémové a trvalé protinádorové imunitě.
Vývoj OV se zaměřuje na dvě hlavní oblasti: bezpečnost a účinnost.
Bezpečnost použití OV
Bezpečnost použití onkolytických virů (OV) je důležitým faktorem při jejich vývoji a klinickém použití. Onkolytické viry se od standardních léčiv značně liší tím, že jsou to živé viry, které se při klinickém podání množí. To může vést k proměnlivým účinným dávkám a proces ztěžuje stanovení dávek, které jsou bezpečné a zároveň účinné. Historicky byly vybírané onkolytické viry, které se zdály být účinné v protinádorové léčbě, ale způsobovaly sekundární infekce nebo komplikace spojené s infekcí OV. Při dalším vývoji se vybírají lidské viry s minimálním patogenním potenciálem pro člověka, například orthoreoviry, nebo veterinární patogeny, jako je virus newcastleské choroby kuřat (NDV) nebo virus vezikulární stomatitidy (VSV). Původní patogenita viru však nemusí být nepřekonatelnou překážkou.
Pokud jsou známy mechanismy, kterými virus vyvolává nemoc, je možné pomocí genového inženýrství odstranit nežádoucí vlastnosti viru. To platí pro mnoho OV, které se v současnosti používají v klinických studiích. Obecně však platí, že čím více se zvyšuje bezpečnost virových vektorů pomocí manipulací, tím více se snižuje jejich účinnost. Při replikaci viru v těle pacienta může být také riziko proměnlivosti, což přináší významná rizika a komplikace. Není tedy překvapivé, že i přes velké množství různých OV, které procházejí preklinickým hodnocením a první fází klinického hodnocení, je v současné době ve fázích II-IV klinických studií zaregistrovaný jen relativně úzký okruh virů.
Zlepšování účinnosti OV
Při vývoji onkolytických virů (OV) se zaměřujeme na zlepšení jejich účinnosti. Toho lze dosáhnout následujícími způsoby:
- Transdukční cílení OV: Snahou je zajistit, aby virus selektivně vstupoval do nádorových buněk. To umožňuje preferenční infekci nádorových buněk a minimalizuje infekci zdravých buněk.
- Transkripční cílení OV: Cílem je dosáhnout selektivní aktivace replikace viru pouze v nádorových buňkách. Toho lze dosáhnout například vložením specifických promotorů, které jsou aktivováné pouze v nádorovém prostředí.
- Vyzbrojení OV: Pro posílení onkolytického a imunoterapeutického potenciálu viru se do něj doplňují transgeny. Tyto transgeny mohou kódovat například cytokiny nebo proteiny, které zesilují účinek viru v boji proti nádorovým buňkám.
- Akumulace OV v nádorech při systémovém podání: Cílem je dosáhnout preferenční akumulace viru v nádorové tkáni i při systémovém podání. Toho lze dosáhnout úpravou vlastností viru nebo využitím faktorů specificky přítomných v nádorovém prostředí.
Schopnost OV množit se v nádorových buňkách je ovlivněna různými mechanismy, které se podílejí i na běžné virové infekci a nazývají se virový tropizmus. Virový tropizmus je určený rozpoznáváním buněčných receptorů umožňujících vstup viru do buňky, přítomností hostitelských faktorů nezbytných pro replikaci viru a nastavením antivirové signalizace v buňce, která se může lišit mezi různými buňkami a tkáněmi.
Některé viry přirozeně využívají receptory, které jsou nadměrně exprimované na nádorových buňkách. Předpokládá se, že selektivní množení těchto virů v nádorech je především způsobené specifickostí těchto receptorů. Příkladem může být virus spalniček, který využívá pro vstup do buněk receptor CD46. U nádorových buněk je tento receptor nadměrně exprimovaný, až 14krát více než u normálních buněk, a klinická i experimentální data potvrzují jednoznačnou souvislost mezi zvýšenou expresí CD46, maligní transformací a metastatickým potenciálem. Nádorové buňky s nadměrnou expresí tohoto receptoru jsou tedy náchylné k infekci a onkolýze vakcinačním kmenem spalniček, stejně jako některými typy adenovirů, které také využívají receptor CD46.
Selektivita jiných virů vůči nádorovým buňkám souvisí s tím, že imunitní odpověď v těchto buňkách často není správně regulovaná. Například aktivace onkogenu RAS vede k selhání hlavní interferonové protivirové obrany založené na proteinkináze aktivované dvouvláknovou RNA (PKR). To vysvětluje, proč se typicky reoviry, které mají dvouvláknovou RNA, úspěšně množí a šíří v nádorech s aktivovaným onkogenem RAS, zatímco v normálních zdravých buňkách je infekce díky aktivní PKR potlačená již v počátečních fázích. U jiných přirozeně onkolytických virů však zatím není plně objasněná podstata jejich nádorového tropismu. Z uvedeného vyplývá, že tropizmus viru je fenomén, se kterým lze při vývoji OV pracovat, a to tím lépe, čím důkladněji jsou prostudovány mechanizmy virové infekce konkrétního viru a charakteristiky nádorových buněk (tkání), na které chceme OV zacílit.
Transdukční cílení na nádorové buňky
Při vývoji onkolytických virů (OV) není nutné spoléhat pouze na přirozenou receptorovou specificitu. Pseudotypování virů je jedním ze způsobů, jak ovlivnit tropismus viru. Pseudotypování umožňuje, že genom jednoho viru je uzavřen v kapsidě nebo obalu druhého viru, což vytváří pseudotyp s novými povrchovými virovými proteiny. Tímto způsobem mohou být transdukovány buňky, které byly dříve nedostupné. Pseudotypování se stalo standardním nástrojem ve virologii pro změnu, rozšíření nebo zúžení virového tropismu. Pro experimentální účely a vývoj OV je využívaný k zaměření na nádorové receptory.
Další možností je vytváření chimérických virů, které zachovávají stávající povrchové charakteristiky, ale jsou obohacené o nové vlastnosti z jiného viru. Sofistikované úpravy kapsidových proteinů nebo obalových glykoproteinů také umožňují přesměrování OV na nádorové receptory. Peptidové ligandy s vysokou afinitou pro nádorové receptory nebo protilátky, nalezené v peptidových nebo protilátkových knihovnách, mohou být využité k zaměření léčiv a virů na nádorové receptory. Genovým inženýrstvím lze tyto peptidy nebo jednořetězcové variabilní části (scFv) protilátek inkorporovat do povrchových struktur viru, což zvyšuje transdukci OV do vytipovaných nádorů. Chemické připojení ligandů a scFv na virové částice je také možné, ale dosud se nedočkalo žádného klinického použití, protože je výrobně náročné.
Transkripční cílení OV
Transkripční cílení onkolytických virů (OV) využívá charakteristických vlastností nádorových buněk, jako je aberantní exprese povrchových molekul a celková deregulace signálních drah. Tato deregulace je spojená s aktivací onkogenů a deaktivací nádorových supresorových genů, což vede k nekontrolované proliferaci a imunitnímu úniku buněk. Těchto vlastností lze využít při hledání a optimalizaci kandidátních OV.
Jako příklad zmíníme konstrukce onkolytického viru odvozeného od adenoviru (Ad), který se množí pouze v buňkách s nefunkčními regulátory buněčného cyklu, proteiny RB a p53. Odstraněním části genů E1A nebo E1B v genomu Ad vzniká onkolytický Ad (oAd), který se replikuje pouze v nádorových buňkách s nefunkčními regulátory buněčného cyklu. Tento přístup byl využit při konstrukci oAd ONYX-015, který byl úspěšně klinicky testovaný u nádorů s defektem v p53 a stal se prvním schváleným OV v Číně. Podobně jsou navrhovány oAd cílící na nádory s defektem RB.
Variací tohoto přístupu je vložení nádorově specifického promotoru před oblast E1A a E1B genů. To způsobuje, že upravený oAd produkuje klíčové regulační proteiny pouze v buňkách, kde je nádorově specifický promotér aktivovaný. Příkladem takového oAd je Telomelysin (OBP-301) – Ad, který má E1A a E1B oblasti pod kontrolou telomerázového promotéru. Telomelysin prochází klinickými testy v kombinovaných terapiích pro léčbu dětského retinoblastomu, rakoviny pankreatu a nádorů hlavy a krku.
Vyzbrojení OV
Princip účinku onkolytických virů (OV) spočívá nejen v selektivní lytické replikaci v nádorových buňkách, ale také v jejich schopnosti ovlivnit imunosupresivní mikroprostředí nádoru. Pro zvýšení jejich účinnosti lze OV vybavit různými geny, které kódují imunomodulační molekuly, jako jsou cytokiny, chemokiny, bispecifické protilátky aktivující T-lymfocyty (BITE), inhibitory imunitních kontrolních bodů, tumor-specifické antigeny (TSA) nebo chimérické antigenní receptory T-lymfocytů (CAR-T).
Cytokiny
Cytokiny jsou molekuly zprostředkující komunikaci mezi buňkami imunitního systému a mohou mít protinádorové účinky. Pro dosažení požadovaného efektu v nádoru je však často potřeba použít vysoké dávky cytokinů, což může být spojeno s významnou toxicitou. Řešením je lokalizovaná exprese cytokinů přímo v místě nádoru pomocí OV vybavených geny pro cytokiny. Mezi často používané geny patří geny pro lidský GM-CSF, interleukiny (IL)-2, IL-12, IL-1 nebo interferony (IFN)-a, IFN-b nebo IFN-g. Řada těchto ozbrojených OV je aktuálně testována v klinických studiích.
Chemokiny
Chemokiny jsou malé proteiny, které slouží jako chemické atraktanty pro leukocyty a mohou přispět k transformaci imunologicky chladného nádoru na místo, které přitahuje efektorové T-lymfocyty. Intratumorální exprese chemokinů pomocí kandidátních ozbrojených onkolytických virů (oAd) byla experimentálně ověřená pro různé oAd. Jedním z aktuálně probíhajících klinických testů je oAd NG-641, který exprimuje CXCL9, CXCL10, IFN-a a také bispecifickou protilátku (BITE) FAP-Tac, která navádí T-lymfocyty na fibroblasty asociované s nádory (FAP-Tac BITE).
Expresí BITE se oAd NG-641 stává velmi zajímavým, protože BITE jsou schopné aktivovat T-lymfocyty, které nemají specifický T-buněčný receptor (TCR) a nevyžadují exprese antigenu hlavního histokompatibilního komplexu (MHC) na cílových buňkách. Systémové podávání BITE je však limitované jejich krátkým poločasem rozpadu a vyžaduje vysoké dávky s potenciální nežádoucí toxicitou. Navíc je účinek BITE omezený, protože aktivovatelné T-lymfocyty se v solidních nádorech obvykle vyskytují jen v omezené míře nebo vůbec.
Lokální exprese bispecifických protilátek (BITE)
Lokální exprese bispecifických protilátek (BITE) s pomocí ozbrojených onkolytických virů (OV), které způsobují infiltraci T-lymfocytů do nádorů, je atraktivní strategií léčby. V minulosti proběhlo několik studií s různými OV, včetně viru vakcinie, Ad, viru spalniček a HSV-1, které používaly BITE s povzbudivými výsledky. OV NG-641, který je v současnosti testovaný klinicky, využívá BITE namířené na buňky nádorového stromatu, nikoli přímo na nádorové buňky. NG-641 je tedy multimodálním agensem, který způsobuje virolýzu nádorových buněk a aktivaci endogenních T-lymfocytů, které útočí a ničí stromální fibroblasty. Klinické studie s NG-641 provádí společnost PsiOxus Therapeutics Ltd (Velká Británie), která se specializuje na OV ovlivňující nádorové mikroprostředí.
Inhibitory imunitních kontrolních bodů
Inhibitory imunitních kontrolních bodů (immune checkpoint inhibitors - ICIs) představují průlom v imunoterapii nádorů, ale přínos z této terapie je omezen na 20 – 40 % pacientů s imunologicky „horkými“ nádory. Kombinace OV, které mají schopnost senzitizovat nádory imunologicky, a ICIs se jeví jako logický přístup. Klinické studie zkoušejí podávání ICIs a OV odděleně v různých schématech, ale také se vyvíjejí ozbrojené OV obsahující geny pro ICIs. Výsledky zatím naznačují, že tento přístup může být účinnější než kombinovaná terapie za určitých okolností.
Tumor-specifické antigeny (TSA)
Nádory produkují řadu růstových faktorů, které posilují imunosupresivní prostředí. Geny inhibující tyto růstové faktory se staly kandidáty pro konstrukci ozbrojených onkolytických virů (OV). Byly vyvinuté OV, které exprimují receptor pro transformující růstový faktor beta (TGF-b) nebo protilátku proti vaskulárnímu endoteliálnímu růstovému faktoru (VEGF). Tyto ozbrojené OV prokázaly lepší onkolytické účinky než neozbrojené varianty. U některých nádorů může nedostatečná exprese nádorově specifických neoantigenů být důvodem, proč nádory unikají imunitnímu systému. Teoreticky by mohly být OV využity pro vnášení tumorově specifických antigenů (TSA). Experimenty na myším modelu ovariálního nádoru s onkolytickým rhabdovirem Maraba exprimujícím modelový antigen ukázaly, že je třeba kombinovat různé terapeutické intervence (očkování, booster OV a následná blokace PD-1 receptoru) pro částečný úspěch tohoto přístupu.
Onkolytické viry (OV) mohou být vybavené cílovými molekulami pro CAR-T buňky, což jsou geneticky upravené T-lymfocyty používané k léčbě některých typů nádorů. Schválením prošlo několik preparátů, které využívají CAR-T buňky zaměřené na CD19 marker B-lymfocytů pro léčbu B-lymfomů. Nicméně tato terapie není účinná při léčbě solidních nádorů, pravděpodobně kvůli nedostatečnému nebo heterogennímu exprimování nádorových antigenů. Proto se nabízí možnost využít onkolytických virů k vyvolání exprese těchto antigenů v solidních nádorech.
Léčba by probíhala dvouetapově, nejprve by byl použitý ozbrojený OV, který by vyvolal exprese nádorových antigenů, a poté by byla aplikovaná terapie pomocí CAR-T buněk zaměřených proti těmto antigenům. Zatím neexistují klinická pozorování, která by potvrdila účinnost tohoto konceptu, ale výsledky na myším modelu melanomu jsou povzbudivé. Použitím vakcíny OV, která vyvolala exprese CD19 molekuly v nádorových buňkách, se podařilo pomocí CAR-T buněk zaměřených proti CD19 prodloužit medián celkového přežití o 50 % oproti kontrolním skupinám.
Výběr OV pro klinické využití
Mezi často používané onkolytické viry (s možností úprav) patří lidské orthoreoviry, lidské pikornaviry, paramyxoviry, ptáčí paramyxoviry nebo potkaní parvovirus H1. Geneticky upravené viry, zejména oAd a OV odvozené od viru vakcínie a lidských herpesvirů, jsou také v klinickém testování významně zastoupené. Ad vektory mají vynikající bezpečnostní profil, stabilitu a lze je připravovat ve vysokých titrech. Jsou genetickou platformou, která umožňuje úpravy pro optimalizaci použití v genové terapii, vývoji vakcín nebo rozvoji onkolytického potenciálu. ONCOS-102 je příkladem aplikace principů zvyšování účinnosti onkolytických virů. Je vytvořený na základě lidského Ad sérotypu 5, ale jeho kapsida nese vazebnou doménu sérotypu 3, což eliminuje inaktivaci viru protilátkami. Obsahuje také gen pro GM-CSF, který zvyšuje protinádorovou imunitní odpověď po aplikaci.
Velkou skupinu onkolytických virů v klinických studiích tvoří viry odvozené od viru vakcínie. Jedná se o poxvirus, který byl historicky používaný jako očkovací látka proti neštovicím. Virus vakcínie se také využívá jako virový vektor pro genové terapie, díky dobře zvládnuté technologii manipulace. Retrovirové replikativní vektory mají unikátní postavení, protože se integrují do genomu hostitelské buňky a způsobují perzistentní infekci. Replikativní retrovirové vektory jsou selektivní pro nádorové buňky a získávají onkolytický potenciál pomocí transgenu označovaného jako „sebevražedný gen“. Tento gen přeměňuje netoxické látky na toxická chemoterapeutika, což způsobuje „sebevraždu“ infikovaných buněk, zatímco nenádorové buňky nejsou ovlivněny.
Schválené komerční přípravky pro onkolytickou viroterapii
Dosud byly celosvětově schválené pouze čtyři preparáty onkolytických virů. Prvním schváleným přípravkem byl preparát Rigvir v Litvě v roce 2004, který se používá pro léčbu melanomů. Rigvir je přírodní onkolytický virus, který nebyl geneticky upravovaný, ale byl adaptovaný na růst v melanomech. Je registrovaný v několika zemích, včetně Litvy.
Druhým schváleným přípravkem byl v roce 2005 v Číně geneticky upravený adenovirus s názvem Oncorine (H-101). Oncorine byl vyvinutý s genetickými úpravami, které umožňují selektivní replikaci viru pouze v nádorových buňkách s defektem v genu p53. Na stejném principu byl dříve v USA vyvíjen oAd ONYX-015, na který koupila firma Shanghai Sunway Biotech Co. Ltd. všechna licenční práva.Tento geneticky upravený adenovirus je schválený pro léčbu nádorů hlavy a krku ve spojení s chemoterapií a probíhají také klinické testy pro další indikace.
Třetím schváleným onkolytickým virem je talimogene laherparepvec (T-VEC nebo Imlygic), který je schválený pro léčbu recidivujícího maligního melanomu. Tento virus, odvozený z HSV-1, byl geneticky upravený tak, aby se selektivně množil v nádorových buňkách a byl do něj vložený gen GM-CSF pro protinádorový efekt. T-VEC procházel klinickými zkouškami pod názvem OncoVEXGM-CSF.
Posledním schváleným onkolytickým virem je DELYTACT (teserpaturev/G47Δ), geneticky upravený HSV-1, který je schválený pro experimentální léčbu nádorů mozku v Japonsku. Tento virus se replikuje pouze v nádorových buňkách díky genetickým úpravám, které odstranily určité geny. DELTYACT je geneticky upravený HSV-1 s další mutací v genu α47. Tato mutace vede k stimulaci lymfocytů v nádoru a zvýšení replikace viru. DELYTACT prošel preklinickými testy, které prokázaly jeho bezpečnost a silnou protinádorovou účinnost. Klinické studie potvrdily účinnost při léčbě glioblastomů a nyní se zkouší i pro léčbu nádorů prostaty, okulárních neuroblastomů a maligního pleurálního mezoteliomu. Experimentálně se také zkouší kombinace tohoto viru s imunitními kontrolními body (ICIs).
